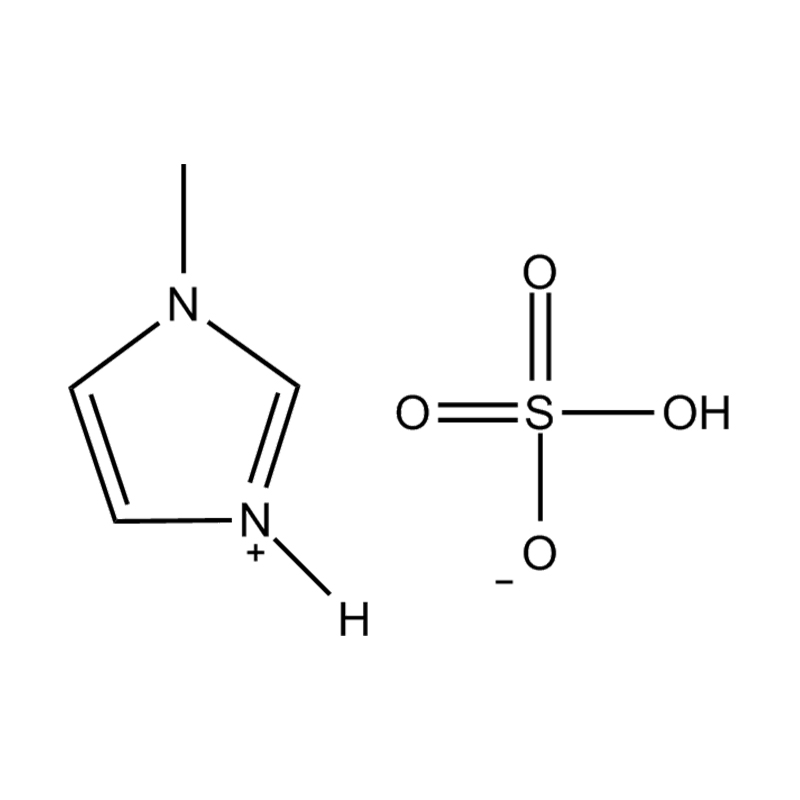
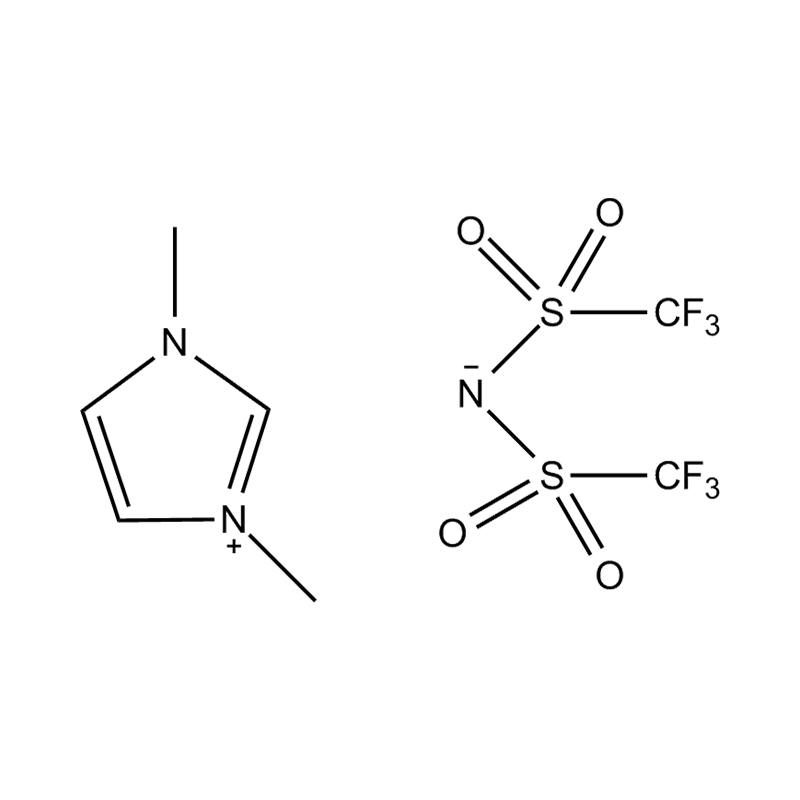
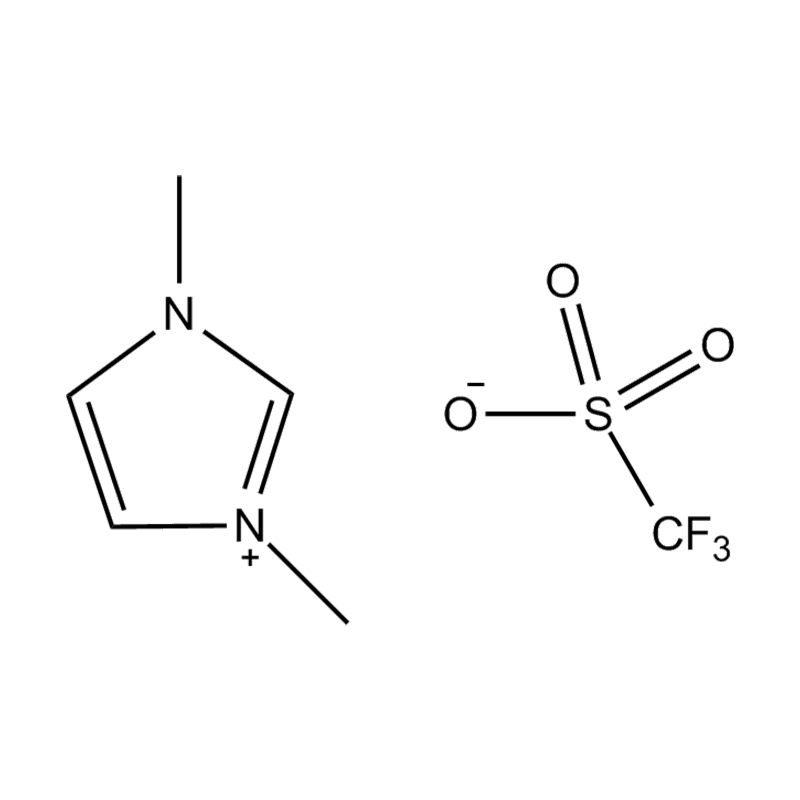
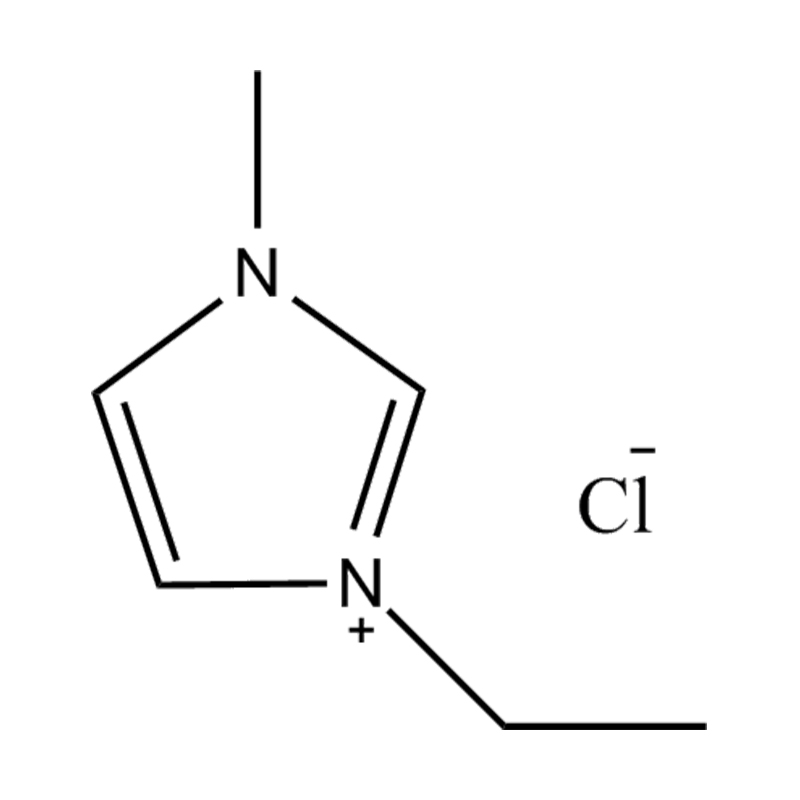
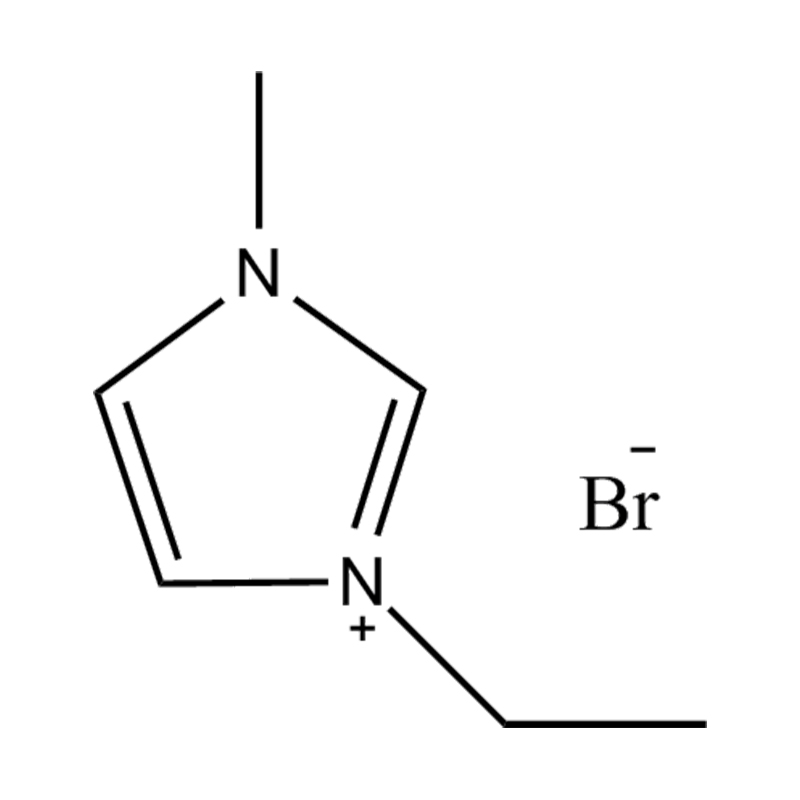
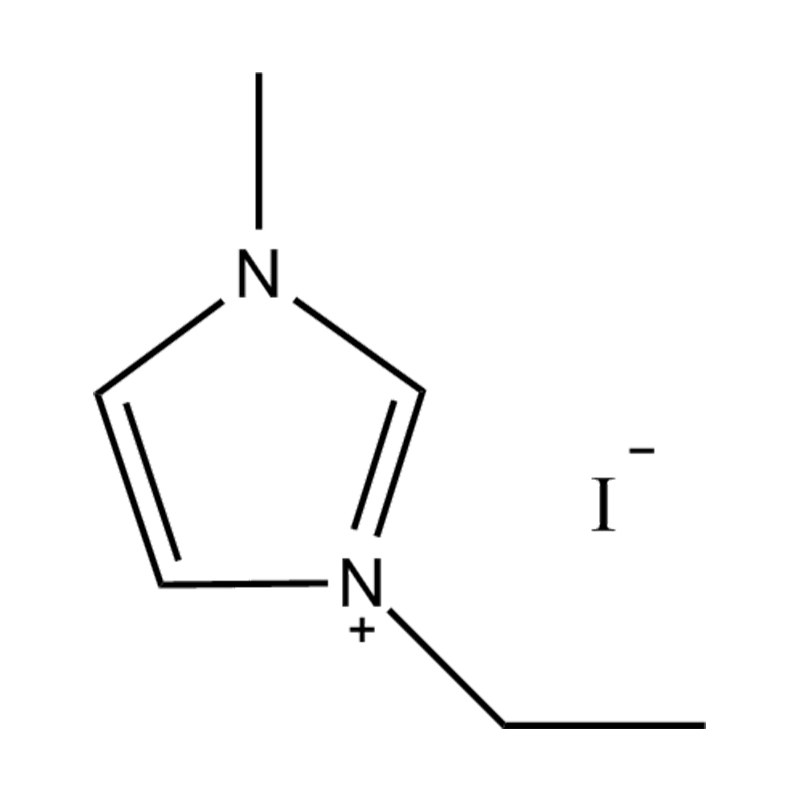
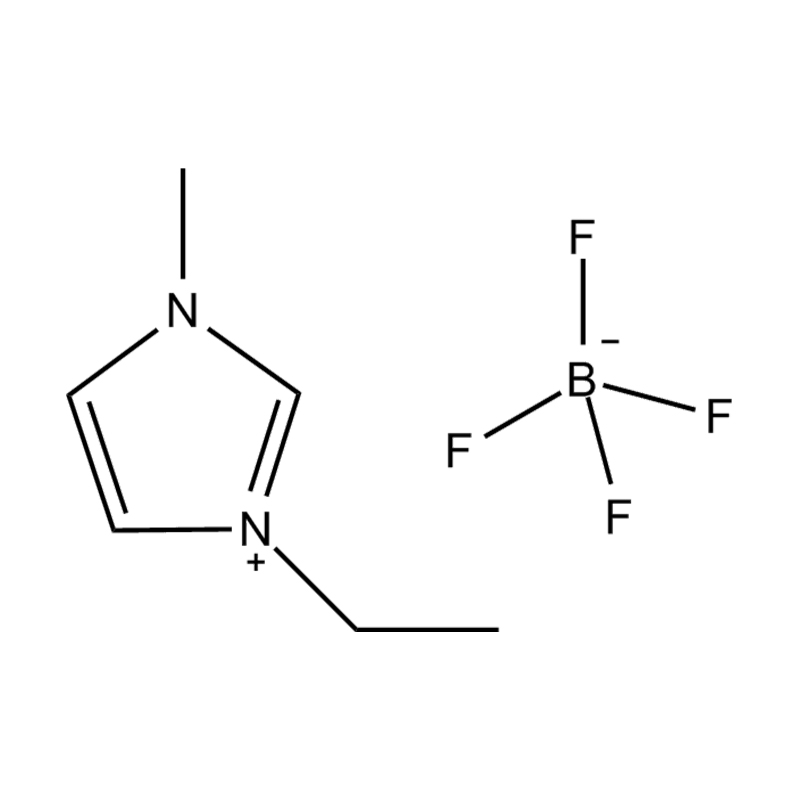
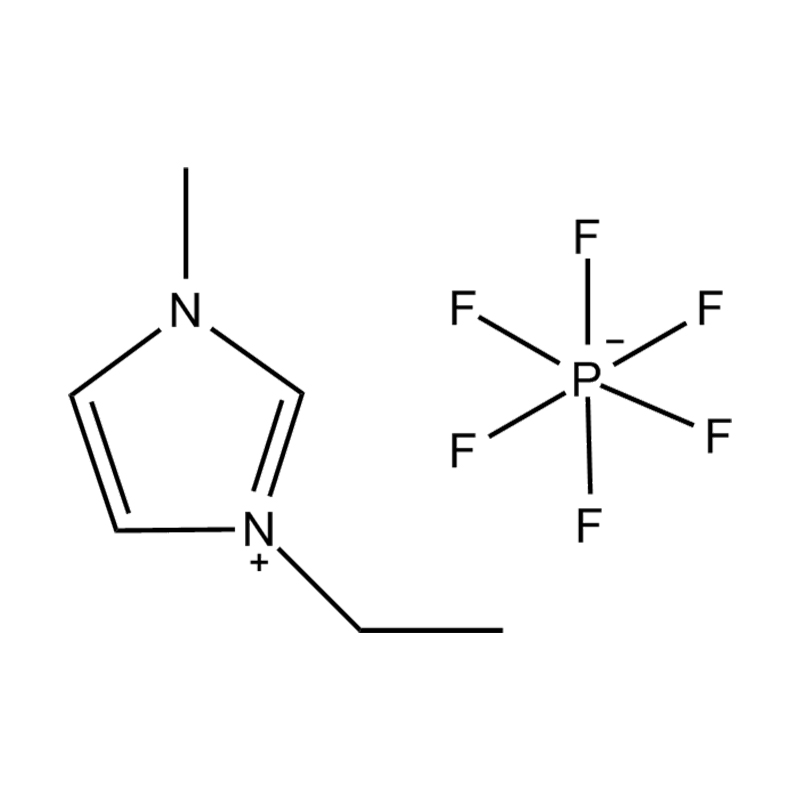
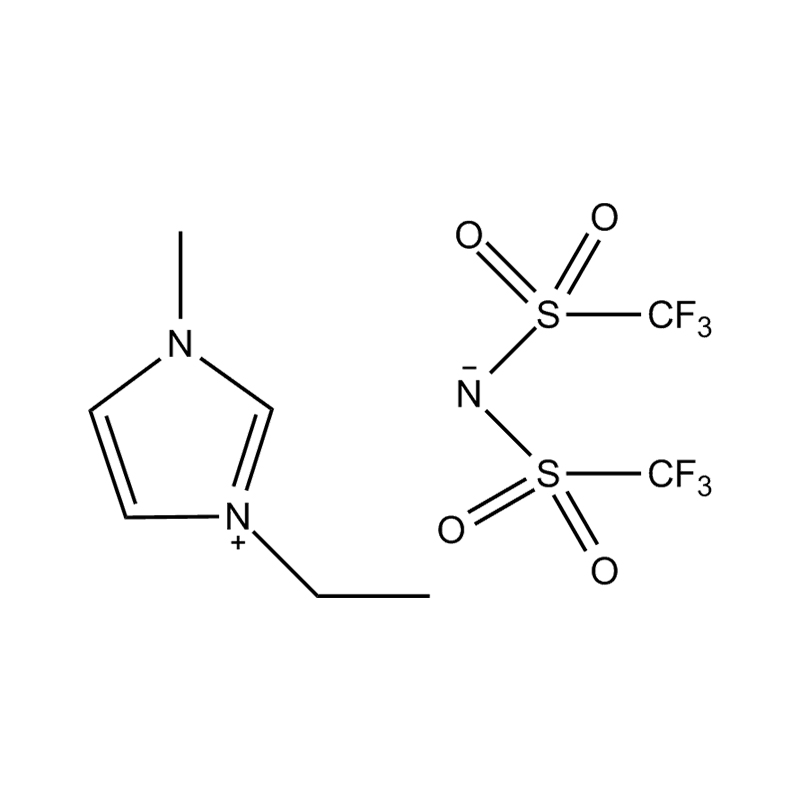
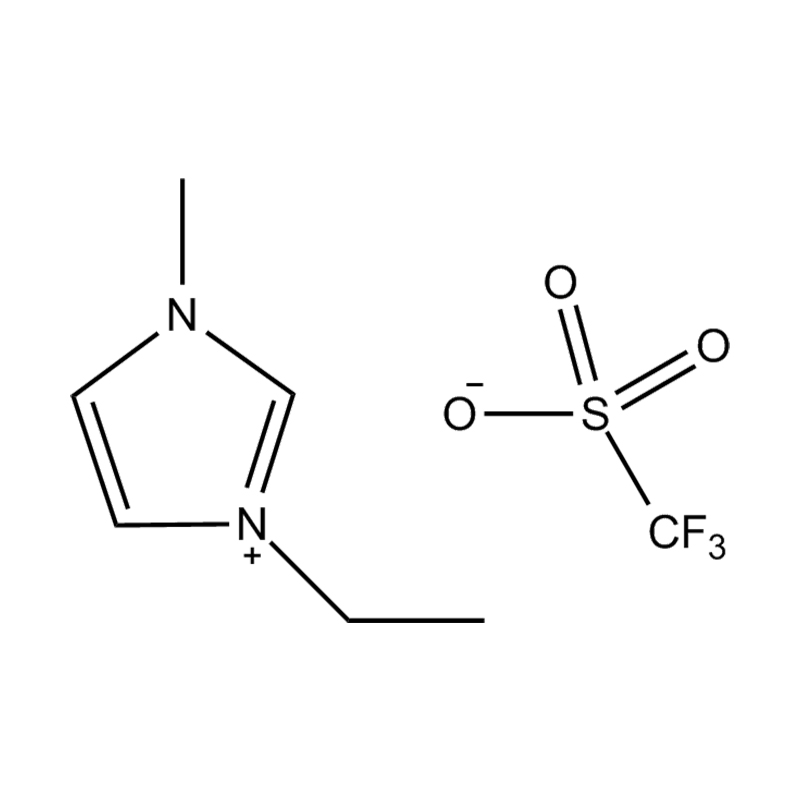
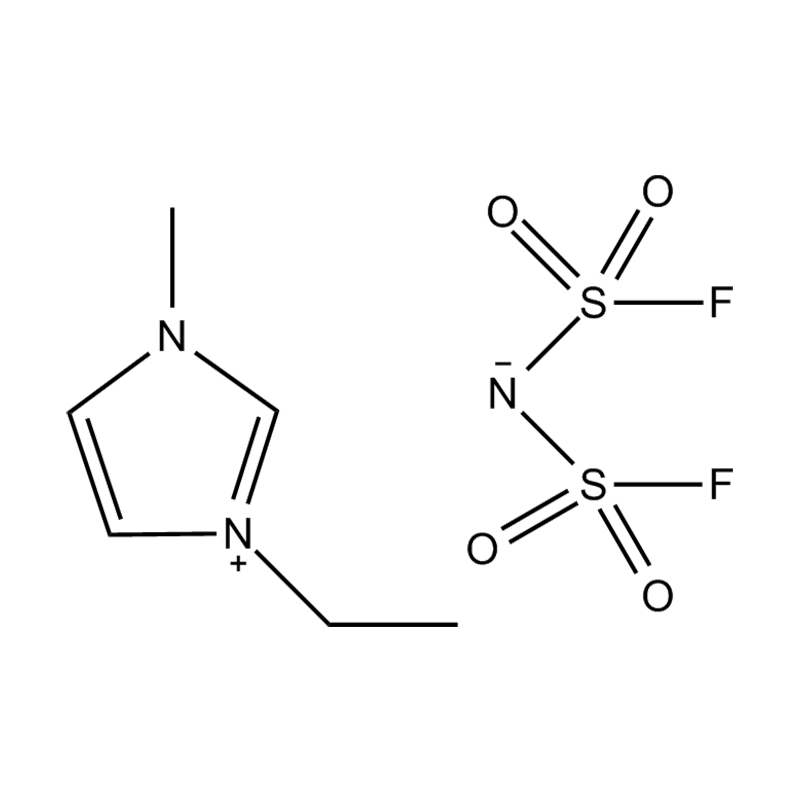
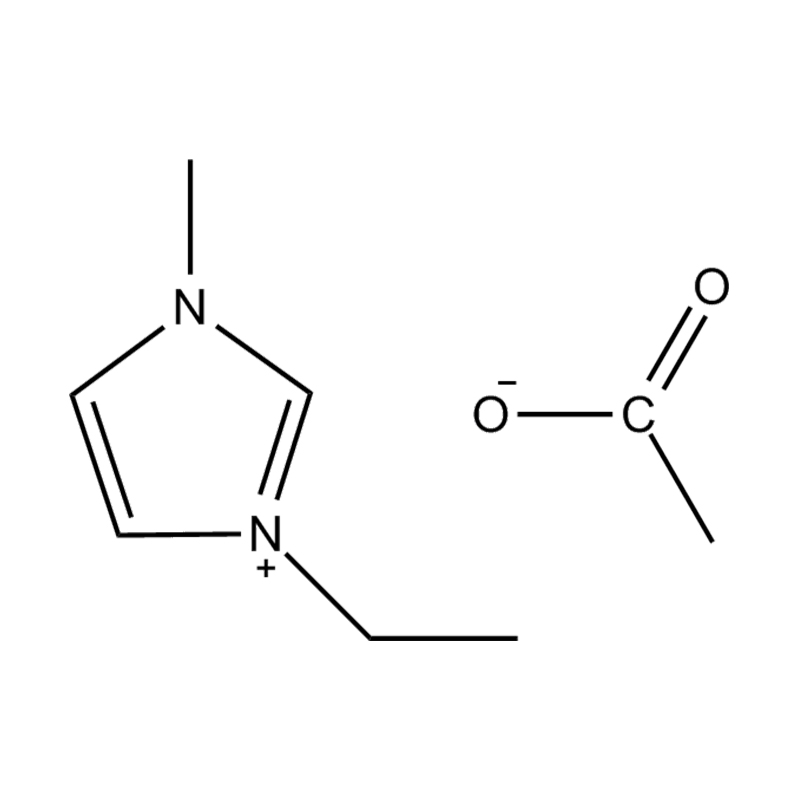
Stabilitatea electrochimică a lichide ionice imidazol imidazol În mediile de înaltă tensiune sau redox-activ este influențat de mai multe mecanisme interrelaționate înrădăcinate în structura lor moleculară și configurația electronică:
Delocalizarea electronilor pe inelul imidazol: natura aromatică a inelului imidazol permite delocalizarea semnificativă a electronilor π, ceea ce îmbunătățește rezistența moleculei la degradarea oxidativă sau reductivă. Atunci când este înlocuit atât la pozițiile 1 și 3, densitatea electronică poate fi redistribuită într-un mod care stabilizează cationul împotriva reacțiilor de transfer de electroni.
Efecte substituente: tipul și poziția substituenților asupra inelului imidazol afectează semnificativ stabilitatea electrochimică. Grupurile donatoare de electroni pot îmbunătăți nucleofilicitatea și pot reduce stabilitatea oxidativă, în timp ce grupurile de retragere a electronilor (cum ar fi halogeni sau nitrile) pot îmbunătăți rezistența oxidativă prin stabilizarea orbitalului molecular cel mai ocupat (HOMO). În schimb, aceste grupuri pot scădea, de asemenea, potențialul de reducere prin stabilizarea celui mai mic orbital molecular neocupat (LUMO), în funcție de mediu.
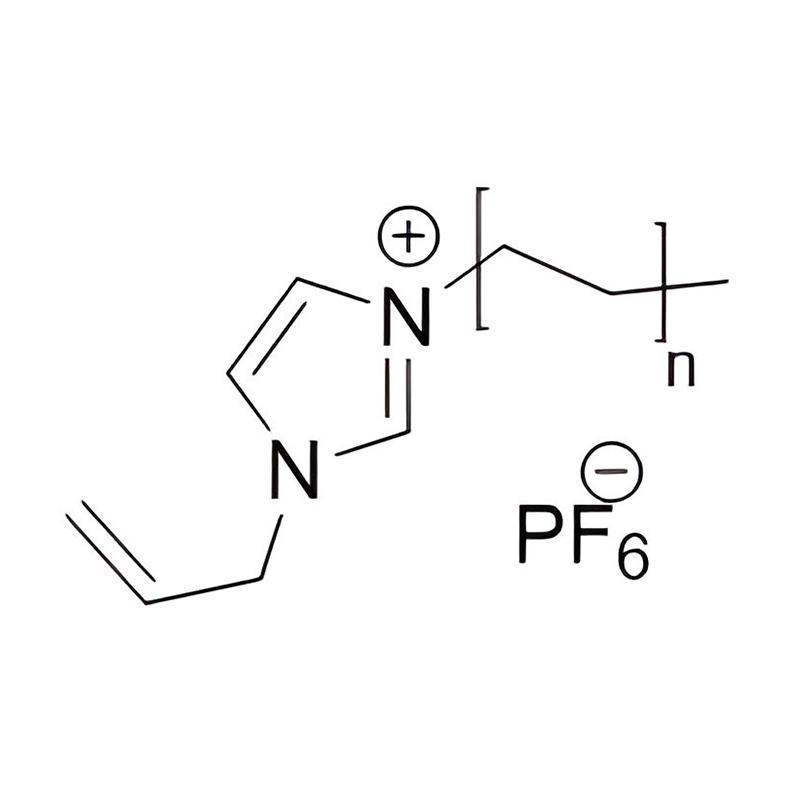
Împărțirea sterică și protejarea spațială: substituenții voluminoși la pozițiile 1 și 3 pot proteja fizic inelul de imidazolium de atacul nucleofil sau electrofil, limitând reacțiile laterale nedorite care ar putea apărea în condiții de înaltă tensiune.
Stabilitatea perechii de anion-cation: împerecherea cationului de imidazolium disubstituit cu un anion stabil, care nu coordonează (de exemplu, bis (trifluorometilsulfonil) imide [tfsi⁻] sau tetrafluoroborat [bf₄⁻]) reduce probabilitatea reacțiilor secundare și contribuie la un fereastră electrochemic. Acești anioni rezistă la descompunere și mențin conductivitatea ionică fără a interfera în reacțiile redox.
Mobilitatea ionică și comportamentul interfațial: în sistemele de înaltă tensiune, în special în dispozitivele electrochimice, mobilitatea ionilor și organizarea acestora la interfețele electrodului influențează stabilitatea. Lichidele ionice imidazol disubstituite pot forma straturi interfațiale bine organizate care împiedică transferul direct de electroni între electrod și speciile ionice, îmbunătățindu-și fereastra electrochimică.
Stabilitatea termică și căile de descompunere: Stabilitatea termică intrinsecă a structurii imidazol disubstituite minimizează riscul de descompunere termică sub stres electrochimic, care este adesea însoțit de degradarea indusă de tensiune.



 中文简体
中文简体